Capítulo 45. Homeostasis III: la respuesta inmune
Los animales de diferente complejidad
presentan una diversidad de respuestas que excluyen o destruyen a los microorganismos,
a otros invasores extraños y a células que no son típicamente
propias. Estas respuestas dependen de una variedad de tipos de leucocitos, todos
los cuales son la progenie de las células madre que se autogeneran en
la médula ósea.
La llamada respuesta inflamatoria
no específica implica la liberación de histaminas y otras sustancias
químicas que provocan distensión de los capilares sanguíneos,
un incremento local de la temperatura y la movilización de granolucitos
fagocíticos y de macrófagos al sitio de la infección.Los
interferones proveen otro tipo muy diferente de defensa no específica,
dirigida contra los virus. Son proteínas de bajo peso molecular producidas
por células infectadas por virus que estimulan a las células vecinas
a defenderse contra la infección viral; también estimulan a las
células que intervienen en la respuesta inmune.
La respuesta inmune es altamente
específica e involucra dos tipos de células: los linfocitos B
y los linfocitos T. Cuando los responsables de la respuesta inmune son los linfocitos
B se dice que la respuesta inmune es humoral. En cambio, si los linfocitos responsables
de la respuesta efectora son los linfocitos T, la respuesta inmune es celular.
Los linfocitos B son los protagonistas
principales de la formación de anticuerpos. Los anticuerpos son grandes
moléculas de proteína cuyos sitios de unión son complementarios
de moléculas extrañas llamadas antígenos. La combinación
del antígeno y el anticuerpo inmoviliza al invasor, destruyéndolo
o volviéndolo susceptible a la fagocitosis . Se conocen cinco clases
de anticuerpos -o inmunoglobulinas-, de los cuales las IgG circulantes son las
más intensamente estudiadas.
El modelo aceptado de la formación
de anticuerpos es la llamada teoría de la selección clonal.
Los linfocitos T, que se diferencian
y maduran en el timo, son responsables de la inmunidad mediada por células.
Existen varios tipos de linfocitos T que se distinguen por el tipo de glucoproteína
que portan en su superficie: las células T colaboradoras, las T citotóxicas
y las T supresoras.
Existen abundantes evidencias
que sugiere que el cáncer puede inducir una respuesta inmune y que lo
hace habitualmente. Las células cancerosas son muy similares a las células
normales de un individuo. Sin embargo, dentro del cuerpo actúan como
organismos extraños, con un crecimiento celular desrregulado, invadiendo
y "sofocando" a los tejidos normales o compitiendo con ellos. Es importante
conocer los mecanismos por los que el sistema inmune responde a las células
tumorales de manera de poder establecer estrategias que permitan un rechazo
efectivo de estas células.
Los tejidos y órganos
trasplantados entre individuos que no sean gemelos idénticos provocan
una respuesta inmune por parte de las células T citotóxicas, lo
que puede llevar al rechazo del órgano trasplantado. El éxito
de estos trasplantes se ha incrementado dramáticamente con el desarrollo
de pruebas de antígenos del complejo mayor de histocompatibilidad. Esto
asegura un ajuste más íntimo entre el dador del órgano
y el receptor, y el uso de drogas inmunosupresoras selectivas como la ciclosporina.
De modo semejante, las transfusiones sanguíneas pueden provocar una respuesta
inmune, por los anticuerpos circulantes, a los antígenos A y B que se
encuentran en la superficie de los glóbulos rojos. La tipificación
de la sangre comprende, no sólo a los grupos sanguíneos AB0, sino
a otros antígenos de superficie de los glóbulos rojos, tales como
el factor Rh.
Las enfermedades asociadas con
el sistema inmune incluyen alergias, enfermedades autoinmunes causadas por las
respuestas inmunes del individuo a sus propios tejidos, y el SIDA, una enfermedad
infecciosa fatal. El retrovirus responsable del SIDA (virus de la inmunodeficiencia
humana o HIV), invade y destruye las células T colaboradoras, dejando
al sistema inmune de la víctima incapaz para responder a otras infecciones
o a células malignas.
El conocimiento en profundidad
de los mecanismos y acciones llevadas a cabo por el sistema inmune ha permitido
lograr importantes avances terapéuticos. Entre ellos podemos mencionar
un mejor desarrollo de vacunas e importantes logros mediante la aplicación
de terapias génicas en individuos inmunodeficientes.
Diversidad de los sistemas inmunes
Los sistemas inmunitarios más
simples corresponden a los poríferos, especies que pueden distinguir
lo propio de lo no propio, a través de células con actividad fagocítica.
Los invertebrados poseen sistemas inmunes que, pese a su relativa simplicidad,
han permitido a muchas especies sobrevivir satisfactoriamente durante cientos
de millones de años sobre la superficie terrestre.
En los animales con celoma se
encuentran células fagocíticas que por medio de un sistema enzimático
encapsulan partículas extrañas y secretan proteínas solubles,
precursoras de los anticuerpos, con capacidad de reconocer ciertas estructuras.
La evolución no sólo ha conservado muchos de los mecanismos de defensa de los invertebrados, sino que ha resguardado muchas de las señales que controlan tales mecanismos. La inmunología comparada ha podido demostrar que, por ejemplo, los mensajes intercelulares, mediados por proteínas regulatorias -las citoquinas- están presentes en especies como la estrella de mar.

Representación esquemática de las primeras evidencias de la respuesta inmune celular establecidas por Elie Metchnkoff a fines del siglo XIX.
Nótese la presencia de fagocitos rodeando una espina de rosal con la
que el científico ruso pinchó una larva de estrella de mar y,
así, sentó las bases de la actual inmunología celular.
En los vertebrados, estas defensas
han evolucionado produciendo una compleja red de interacciones que implica respuestas
no específicas (como la inflamación), así como las respuestas
altamente específicas del sistema inmune, elaboradas a la medida precisa
de cada invasor diferente.
Un elemento esencial en la defensa
de los vertebrados ha sido la adquisición de "memoria inmunológica",
por lo que el rechazo de lo no propio se realiza con mayor rapidez ante un segundo
contacto con el inductor de la respuesta.
Defensas no específicas
La primera línea de defensa
de la mayoría de los organismos contra invasores extraños es anatómica,
y está constituida por la piel y las membranas mucosas. La piel, con
su capa dura de queratina, es una barrera inexpugnable. Cuando se daña,
gran cantidad de microorganismos pueden entrar rápidamente al cuerpo.
El epitelio que forma las membranas mucosas es más frágil que
la piel, pero constantemente está bañado por fluidos que contienen
sustancias antimicrobianas o por cilios, que barren los microorganismos que
entran al sistema respiratorio. El pH extremadamente ácido de los contenidos
del estómago crea un ambiente inhóspito, y el tubo intestinal
inferior alberga poblaciones residentes de bacterias que defienden su territorio
contra otros microorganismos. A pesar de estas defensas, las membranas mucosas
son los sitios más comunes de entrada de los microorganismos o de sus
toxinas.
Si un microorganismo penetra
la barrera externa, encuentra una segunda línea de defensa que consiste
en una variedad de agentes transportados por la sangre y la linfa circulantes.
La respuesta inflamatoria que se produce, una respuesta local, hace que el área
dañada se hinche y se torne caliente, rojiza y dolorosa.
Tanto la respuesta inflamatoria como la respuesta inmune -una respuesta más específica- dependen de la interacción de una variedad de tipos de glóbulos blancos. Estas células son continuamente sustituidas. Todos los tipos diferentes de glóbulos blancos, al igual que los eritrocitos, resultan de la diferenciación y división de células madre, localizadas en la médula de los huesos largos, que se autorregeneran.
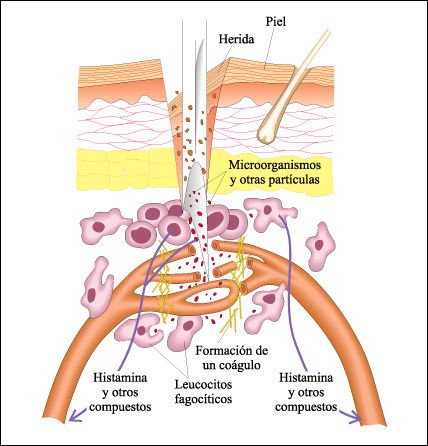
La respuesta inflamatoria.
Barreras de defensa del cuerpo atravesadas por una fragmento de cristal. Las
propias células del cuerpo y las células bacterianas secretan
diversos compuestos químicos que se liberan en el lugar de la herida.
Estas sustancias, entre ellas la histamina, hacen aumentar el flujo de sangre
en la zona, aumentan la permeabilidad de los capilares y atraen a los leucocitos
que migran desde los capilares hacia la herida. Se forma también un coágulo
que da comienzo al proceso de cicatrización. Cuando los leucocitos entran
en escena, fagocitan a los microorganismos y partículas extrañas.
Algunos leucocitos producen una proteína que cambia el valor de referencia
del termostato que está en el hipotalámo produciendo fiebre.
Las principales células
involucradas en la respuesta inflamatoria son los granulocitos o polimorfonucleares,
glóbulos blancos circulantes que se clasifican por sus propiedades de
coloración como neutrófilos, eosinófilos y basófilos.
Los neutrófilos son los
más numerosos. Son capaces de fagocitar a los microorganismos y a otras
partículas extrañas. Contiene lisosomas que participan en la digestión
intracelular. Los basófilos y los eosinófilos también son
fagocíticos. Los basófilos liberan compuestos químicos
como la histamina, que incrementan la respuesta inflamatoria. Los basófilos
participan en las reacciones alérgicas. Un papel clave en estas reacciones
lo desempeñan los mastocitos, basófilos especializados, no circulantes,
que se encuentran en el tejido conectivo.
Los eosinófilos localizan
al agresor agresor y liberan el contenido de sus lisosomas lesionando la membrana
por ejemplo de un parásito y destruyéndolo.
Los monocitos, al igual que
los neutrófilos, son atraídos al sitio de la infección
por compuestos químicos liberados por las células bacterianas
y por las células hospedadoras. Se transforman en macrófagos,
haciéndose más grandes, ameboides y fagocíticos. Los macrófagos
también se alojan en los ganglios linfáticos, el bazo, el hígado,
los pulmones y los tejidos conectivos, donde atrapan a cualquier microorganismo
o partícula extraña que puedan haber superado las defensas iniciales.
También son importantes en la activación de los linfocitos, otros
glóbulos blancos que son los efectores de la respuesta inmune específica.
La respuesta inflamatoria local
está acompañada por una respuesta sistémica -la respuesta
de fase aguda- que se caracteriza por la inducción de fiebre, aumento
de la síntesis de hormonas esteroides y la síntesis de proteínas
hepáticas. Esta respuesta se inicia como consecuencia de la activación
de los macrófagos, quienes secretan mediadores solubles conocidos como
citoquinas proinflamatorias: son las interleuquinas, los interferones y el factor
de la necrosis tumoral.
Estas citoquinas actúan
localmente sobre los fibroblastos y células del endotelio vascular induciendo
la coagulación, modificando la permeabilidad vascular y aumentando la
expresión celular de las denominadas moléculas de adhesión.
Cuando una célula es
invadida por un virus, libera interferón que se une a receptores de las
membranas de las células circundantes. Existen al menos tres clases diferentes
de interferones (a, b y g), todas ellas proteínas pequeñas que
se unen a receptores específicos. Así estimuladas, estas células
producen enzimas que bloquean la traducción del RNA mensajero viral a
proteína y logran así un efecto antiviral. Las moléculas
de interferón estimulan también las respuestas inflamatoria e
inmune.
Los interferones 1) inhiben
la replicación viral, induciendo enzimas que interfieren con el proceso
de replicación viral, 2) activan la función de lisis de las células
infectadas por virus llevada a cabo por los linfocitos denominados NK (natural
killer), 3) favorecen la activación de la respuesta inmune celular específica
(linfocitos T citotóxicos) y 4) al interferir la replicación del
DNA, son capaces de inhibir la proliferación celular.
En la actualidad, los interferones
se producen por medio de estrategias biotecnológicas. Los interferones
recombinantes están siendo utilizados en el tratamiento de infecciones
víricos y de ciertas formas de cáncer.
La respuesta inmune específica
o adaptativa
La respuesta inmune específica
o adaptativa difiere de los otros mecanismos de defensa del cuerpo en que identifica
específicamente al invasor a través de estructuras de la superficie
de un tipo particular de glóbulos blancos, los linfocitos. Cuando los
linfocitos involucrados son los linfocitos B se dice que la respuesta inmune
es humoral. En cambio, si los linfocitos responsables son los linfocitos T,
la respuesta inmune es celular.
La respuesta inmune consta de
una etapa inicial de reconocimiento, una etapa de diferenciación de los
linfocitos específicos que conduce a una tercera etapa efectora en la
cual se ponen en acción una serie de mecanismos de destrucción
del agresor de acuerdo con las características del antígeno.
Cada antígeno estimula
diferentes poblaciones de linfocitos, lo que hace que se desarrollen mecanismos
apropiados que conducen a la eliminacióndel
agresor.
El primer contacto del sistema
inmune con un antígeno inicia la respuesta primaria la que lleva a la
eliminación del invasor y, simultáneamente, provoca la diferenciación
de células que quedan "preadaptadas" a un nuevo contacto con
el antígeno -las células de memoria. En posteriores encuentros
con el mismo antígeno, se produce una respuesta secundaria, más
rápida y de mayor magnitud.
Las respuestas de defensa desarrolladas
por el propio individuo constituyen la inmunidad activa. En ciertas condiciones
fisiológicas (embarazos) o terapéuticas, se produce una transferencia
de los productos de la respuesta inmune, lo que constituye un proceso de inmunidad
pasiva.
La especificidad de la respuesta inmune deriva de las acciones e interacciones de los linfocitos B y los linfocitos T. En los mamíferos, los sitios primarios de diferenciación y proliferación de estas células son la médula ósea (para los B) y el timo (para los T), un órgano esponjoso y bilobulado que se encuentra en la zona superior del tórax. El escenario en que operan estas células se conoce como sistema inmune.
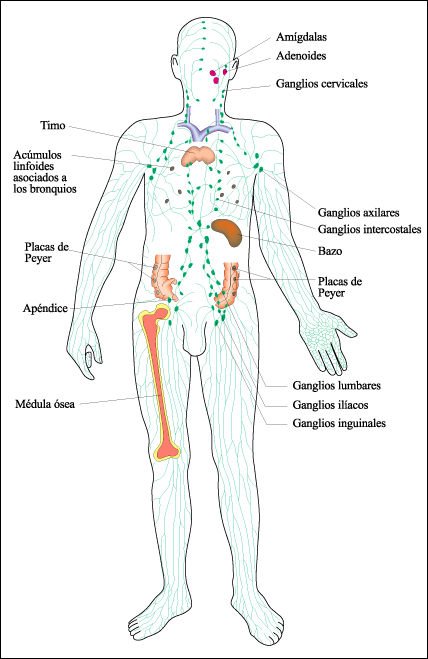
Principales integrantes del sistema inmune humano.
Los principales integrantes del sistema inmune humano son la médula ósea
y el timo, órganos de diferenciación inicial de los linfocitos
B y T, que son los ejecutores de la respuesta inmune. Otros órganos importantes
del sistema son los vasos linfáticos, los numerosos ganglios linfáticos,
el bazo y el sistema asociado a mucosas que incluye a las amígdalas,
el apéndice, las placas de Peyer, las adenoides y los acúmulos
linfoides asociados a los bronquios.
Los vasos del sistema linfático
son la vía de retorno del fluido intersticial al sistema circulatorio.
Dentro de este sistema de vasos están los ganglios linfáticos,
que son masas de tejido esponjoso separadas en compartimientos por tejido conectivo.
Los microorganismos o partículas extrañas y los desechos tisulares
que entran a los espacios extracelulares de cualquier tejido son arrebatados
en el fluido intersticial, barridos a los canales del sistema linfático
y atrapados en los ganglios linfáticos que actúan como filtro.
Los ganglios linfáticos también atrapan a las células bacterianas
y a otros microorganismos. Están densamente poblados por linfocitos y
macrófagos y dentro de estas estructuras ocurren las interacciones esenciales
entre las células que intervienen en la respuesta inmune.
El bazo y el al tejido linfoideo
asociado a mucosas también son ricos en linfocitos y en células
fagocíticas que atrapan partículas. Las amígdalas atrapan
partículas que ingresan por vía nasal o bucal. En la pared del
intestino se encuentran acúmulos de tejido linfoide con folículos
linfoides grandes -las placas de Peyer-, situadas entre el revestimiento interno
de la membrana mucosa y la cubierta muscular externa, y que defienden al resto
del cuerpo contra los miles de millones de microorganismos que habitan el tracto
intestinal normal.
Los linfocitos B y la formación
de anticuerpos
Los linfocitos B son los protagonistas
principales de la respuesta inmune humoral e intervienen en la formación
de anticuerpos, proteínas globulares complejas -conocidas también
como inmunoglobulinas - que presentan en su estructura combinaciones tridimensionales
precisas capaces de interactuar con moléculas que el cuerpo reconoce
como extrañas o no propias.
Algunos linfocitos B "patrullan"
el cuerpo humano y otros son sésiles; se aglomeran en los ganglios linfáticos,
el bazo y otros tejidos linfoides, donde están expuestos a la sangre
y la linfa circulantes. Los linfocitos B son células pequeñas,
redondas, que no se dividen. Insertos en su membrana y, sobresaliendo de su
superficie, se encuentran los anticuerpos con especificidad para reconocer a
un determinado antígeno.
Cuando un linfocito B particular se encuentra en un órgano linfoide con el antígeno para el cual es específico, por complementariedad, los anticuerpos de su superficie interactúan con el antígeno. Esto activa al linfocito B, lo que provoca que la célula se agrande, se divida y que las células hijas -o plasmocitos- adquieran la capacidad de realizar una producción activa de anticuerpos. La proliferación de linfocitos B activados ocurre frecuentemente en los ganglios linfáticos, razón por la cual éstos se agrandan durante una infección. Las células hijas que resultan de la activación de linfocitos B se diferencian en dos tipos, uno de los cuales es la célula plasmática.
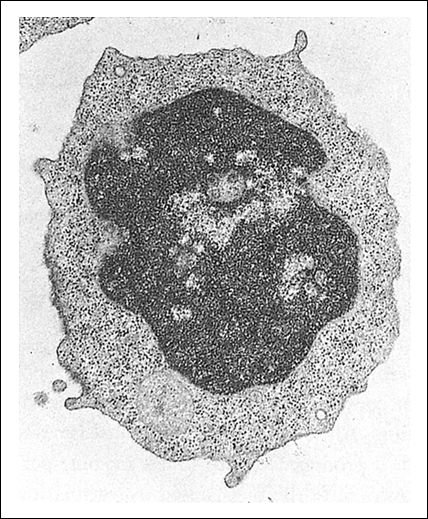
Un linfocito se difrencia a célula plasmática.
a) Un linfocito B activado que se diferencia a célula plasmática
b) Una célula plasmática especializada en la fabricación y secreción de anticuerpos.
El segundo tipo de célula
producido a partir de un linfocito B estimulado por el antígeno son las
células de memoria. Estas células conservan la información
para producir anticuerpos y siguen circulando por largos períodos, incluso
durante la vida completa de un individuo. Así, la segunda vez que un
patógeno en particular entra al cuerpo, inmediatamente puede inducirse
la producción de anticuerpos en gran escala contra el invasor. Esta respuesta
rápida de las células de memoria es la fuente de la inmunidad
a muchas enfermedades infecciosas que ocurre después de una primera infección.
Es también la base para la vacunación contra varias enfermedades.
Los anticuerpos presentes en
los fluidos biológicos tienen la misma estructura que los receptores
para los antígenos presentes en la superficie de los linfocitos B. Estas
glucoproteínas actúan como un adaptador biológico entre
el antígeno y los elementos celulares o humorales responsables de la
destrucción del agresor.
Existe una variedad de mecanismos
efectores en los que participan los anticuerpos: pueden recubrir a las partículas
extrañas y hacer que se aglomeren de modo tal que puedan ser capturadas
por las células fagocíticas; también pueden combinarse
con el agente nocivo e interferir con el mecanismo de penetración celular
de un virus o bacteria. También pueden combinarse con otros componentes
presentes en el plasma -el sistema complemento- y, así, lisar o identificar
a las células extrañas. Finalmente, pueden actuar como nexo entre
una célula infectada o tumoral y las células natural killer para
producir la destrucción a través del mecanismo de citotoxicidad
dependiente de anticuerpos.
Cada anticuerpo es una proteína
compleja que está formada por cuatro cadenas polipeptídicas: dos
cadenas livianas idénticas y dos cadenas pesadas idénticas
Cada una de las cuatro cadenas tiene una región constante (C) -una región común a todos los anticuerpos de su clase- y una región variable (V), que difiere de un anticuerpo a otro. Cuando las cadenas se pliegan, las secuencias variables de aminoácidos se reúnen y forman dos regiones activas de la molécula que se unen a una región determinada del antígeno específico. Se han identificado cinco clases distintas de inmunoglobulinas (IgG, IgA, IgD, IgM e IgE) que se distinguen por las regiones constantes de sus cadenas pesadas.
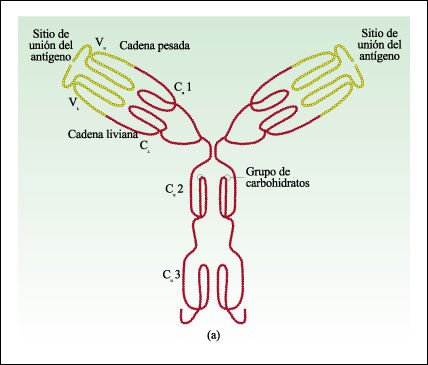
Representación esquemática de una molécula de anticuerpo.
En la representación esquemática de una molécula de anticuerpo
se sugiere de qué manera pueden estar plegadas las cuatro cadenas. Cada
cuenta representa un aminoácido de los cuales hay más de 1.200.
Las regiones variables se muestran en amarillo y las regiones constantes enrojo.
Algunos segmentos de la molécula se pliegan de manera independiente,
conformando los llamados dominiosUno de los hechos más intrigantes acerca
de la respuesta inmune fue, durante mucho tiempo, saber que existe una enorme
variedad de antígenos contra los cuales un solo individuo puede producir
anticuerpos. Se estima que un ratón, por ejemplo, puede formar anticuerpos
contra 10 millones de antígenos diferentes. Además, pueden formarse
anticuerpos, no sólo contra los invasores naturales comunes que un organismo
individual podría encontrar razonablemente durante el curso de su propia
vida, y contra aquellos que sus antecesores podrían haber encontrado,
sino también contra antígenos sintéticos que son químicamente
distintos de cualquier sustancia que se encuentre en la naturaleza.
La interpretación actual
acerca de la formación de anticuerpos se conoce como la teoría
de la selección clonal.
Un linfocito B no estimulado,
con un tipo específico de anticuerpo expuesto en su superficie, encuentra
moléculas de antígeno con una estructura complementaria al sitio
de unión de sus anticuerpos.Los antígenos se unen a los anticuerpos,
poniendo en movimiento una serie de cambios dentro de la célula (activación).El
linfocito B comienza a dividirse y diferenciarse, formando células plasmáticas
y células de memoria. Las células plasmáticas secretan
grandes cantidades de anticuerpos circulantes todos con una especificidad idéntica
a la de los anticuerpos sobre la superficie del linfocito B original. Las células
de memoria que llevan los mismos anticuerpos persisten en la circulación
indefinidamente; ellas secretan anticuerpos sólo después de un
encuentro posterior con el mismo antígeno y de diferenciarse en células
plasmáticas.
De acuerdo con esta teoría,
la diferenciación de los precursores de linfocitos B que ocurre en la
médula ósea, produce una gran variedad de linfocitos B diferentes,
cada uno de los cuales es capaz de sintetizar anticuerpos con una estructura
tridimensional particular para el sitio de unión.
Después de encontrar
un antígeno que se una a los anticuerpos que exhibe en su superficie,
el linfocito B madura y se divide, dando como resultado un clon de células
plasmáticas que sintetizan anticuerpos circulantes contra ese antígeno
en particular. Se producen también células de memoria, que persisten
en el torrente sanguíneo después de la infección y producen
anticuerpos inmediatamente después de una exposición posterior
al mismo antígeno. Esta respuesta de las células de memoria es
la causa de la inmunidad rápida e intensificada que sigue a la vacunación
o a muchas infecciones virales. La capacidad de producir una tremenda variedad
de linfocitos B, cada uno capaz de sintetizar un anticuerpo especifico, es explicada
por el gran número de secuencias génicas que codifican las regiones
variables de los anticuerpos, por la transposición de estas secuencias
génicas en el curso de la diferenciación de los linfocitos, y
por mutaciones somáticas subsiguientes.
Los linfocitos T y la inmunidad
mediada por células
Los anticuerpos circulantes
no son los únicos efectores de la inmunidad. Hay otra categoría
de respuesta inmune altamente específica que se ejecuta por interacciones
célula a célula; en esa respuesta intervienen los linfocitos T
y se conoce como respuesta mediada por células.
Los linfocitos T ejercen su
acción interactuando con otras células eucarióticas, específicamente
las propias células del cuerpo. Funcionalmente se conocen diferentes
poblaciones de linfocitos T. Los colaboradores, los supresores y los citotóxicos
que se diferencian por tener diferentes glucoproteínas de superficie.
Cuando un linfocito T colaborador
reconoce al antígeno, se activa y secreta proteínas como interleuquinas,
interferón g y factor de la necrosis tumoral que tienen acciones reguladoras
de la respuesta inmune.
Los linfocitos T supresores,
a través de la secreción de citoquinas, disminuyen la actividad
de los linfocitos tanto B como T y de los macrófagos.
Los linfocitos T citotóxicos,
luego de reconocer al antígeno, se diferencian en células efectoras
las que posteriormente pueden inducir la muerte celular y/o sintetizar y secretar
proteínas con acción citotóxica para la célula alterada.
Estos linfocitos actúan contra células eucarióticas extrañas
y contra células del cuerpo infectadas por virus u otros microorganismos
de vida intracelular. Así, cuando un virus está multiplicándose
dentro de una célula, está protegido de la acción de los
anticuerpos, sin embargo, su presencia se refleja en la aparición de
nuevos antígenos en la superficie de la célula infectada que hace
posible que los linfocitos T citotóxicos la encuentren y la destruyan.
Los linfocitos T -al igual que
los glóbulos rojos, granulocitos, monocitos y linfocitos B - derivan
de una progenie de células totipotenciales presentes en la médula
de los huesos largos. Dentro del timo se encuentran los precursores de los linfocitos
T que pasan por un proceso complejo de diferenciación, selección
y maduración. La diferenciación implica, entre otras cosas, adquirir
la capacidad para sintetizar diferentes glucoproteínas de membrana, que
determinan tanto su función como su especificidad antigénica.
El primer tipo de glucoproteína
de membrana existe en una de dos formas, conocidas como CD4 y CD8. Las células
T colaboradoras portan la molécula CD4 sobre su superficie, mientras
que las células T citotóxicas y T supresoras portan la molécula
CD8.
La capacidad de los linfocitos T para desempeñar sus funciones depende de otro tipo de molécula de superficie conocida como receptor del linfocito T que consiste en dos cadenas de polipéptidos, cada una con regiones variables y constantes codificadas por genes que, al igual que los de los anticuerpos, se reordenan en el curso de la diferenciación.
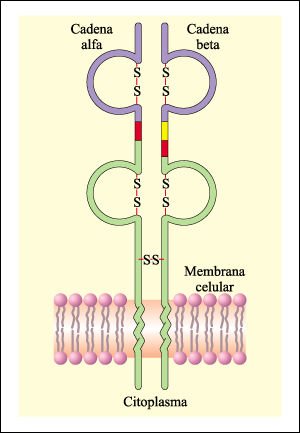
Representación esquemática de la estructura del receptor del linfocito T.
Las cadenas polipeptídicas del receptor del linfocito T, al igual que
las de la molécula de un anticuerpo, están codificadas por genes
que se ensamblan a partir de diferentes componentes. Diferentes porciones de
las cadenas son codificadas por genes variables (violeta), genes para diversidad
(amarillo), genes para unión (rojo) y genes constantes (verde). Las porciones
helicoidales de las regiones constantes que anclan el receptor en la membrana
celular son ricas en aminoácidos hidrofóbicos. El sitio de unión
para los antígenos es una estructura tridimensional compleja, formada
por las regiones variables de las dos cadenas.
El resultado es una enorme diversidad
de linfocitos T, cada uno de los cuales lleva receptores de células con
una sola especificidad antigénica. Los receptores de células T
reconocen y se unen a antígenos determinados genéticamente que
se encuentran en la superficie de las propias células del cuerpo. Estos
antígenos propios están codificados por un grupo de genes conocidos
como el complejo mayor de histocompatibilidad (CMH).
Dos clases de antígenos
CMH participan en la respuesta inmune. Las moléculas de clase I, que
se encuentran en las células de todo el cuerpo, son esenciales para la
identificación de las células enfermas por parte de los linfocitos
T citotóxicos. Las moléculas de clase II se encuentran en la superficie
de los macrófagos y de los linfocitos B. Son esenciales en la presentación
de los antígenos extraños a las células T colaboradoras
que, a su vez, son esenciales para la activación y proliferación
de los linfocitos B y de las células T citotóxicas.
Cuando un agente agresor invade y sobrevive dentro de una célula eucariótica, o cuando se produce alguna transformación celular que modifica las características fenotípicas externas de las células de un individuo, un linfocito T citotóxico es capaz de reconocerlo. El linfocito T puede detectar la combinación de antígeno CMH clase I con los péptidos del antígeno extraño y su receptor se une a esta combinación. El linfocito, entonces, se activa, se diferencia a células citotóxicas maduras y en células de memoria que permanecen en la circulación por tiempo indefinido. Además, las células T citotóxicas activadas liberan citoquinas, que atraen y activan a los macrófagos estimulando la fagocitosis. Las células T destructoras (killer), luego del contacto célula T-célula eucariótica secretan proteínas que destruyen directamente a las células blanco. Así, se moviliza una batería completa de defensas que, mediante la activación de células T citotóxicas, puede conducir a la muerte celular tanto por la inducción de apoptosis como por mecanismos de necrosis celular.
Cuando un virus infecta una
célula eucariótica, se fragmenta dentro del citoplasma, éste
es un paso esencial en la vida del virus, porque libera su ácido nucleico
y le permite comenzar la replicación. Sin embargo, ciertos antígenos
virales que actúan como marcadores aparecen en la superficie de la célula
infectada y son expuestos junto con los antígenos CMH de clase I. Las
células T citotóxicas, cuyos receptores son complementarios de
la combinación antigénica específica que resulta, se unen
a la célula marcada y se activan. Esta activación produce una
proliferación de células T y la diferenciación de las células
hijas en clones de células de memoria y de células T citotóxicas
activas, que luego atacan y destruyen a otras células infectadas. Las
células T activadas también secretan citoquinas que atraen al
área a los macrófagos y a otros glóbulos blancos fagocíticos.
Estas células ingieren los restos de las células lisadas incluyendo
los virus que contenían. Las células de memoria rápidamente
se activan por una segunda exposición a la infección o a un antígeno
extraño.
Cuando una infección
se ha eliminado exitosamente, debe suprimirse la actividad de los linfocitos
B y T. El mecanismo de supresión no ha sido completamente dilucidado
aún. Sin embargo, se sabe que las células T colaboradoras poseen
la capacidad de producir citoquinas con efectos antiinflamatorios e inmunosupresores.
Los estudios sobre la función
de los linfocitos T ha permitido establecer cuál es la red de comunicaciones
celulares que regulan al sistema inmune. Los mediadores solubles producidos
por las células del sistema inmune -las citoquinas- producen interacciones
complejas no sólo con las células del propio sistema sino también
con otros, particularmente, los sistemas endocrino y nervioso. Recíprocamente,
el sistema inmune parece estar influido por las hormonas responsables de la
comunicación intercelular dentro de los sistemas endocrino y nervioso.
El cáncer y la respuesta
inmune
Las células cancerosas,
dentro del cuerpo, actúan como organismos extraños. Presentan
un crecimiento celular desrregulado, invaden a los tejidos normales o compiten
con ellos. Además, virtualmente todas las células cancerosas tienen
en su superficie antígenos que pueden ser reconocidos como extraños.
¿Significa esto que el cuerpo puede montar una respuesta inmune contra
sus propios cánceres?
Aparentemente, no sólo
el cáncer puede inducir una respuesta inmune sino que habitualmente lo
hace. De hecho, habitualmente lo hace exitosamente, dominando al cáncer
antes de que éste se haya detectado.
Pero, si el sistema inmune falla
o las células cancerosas evaden la respuesta instaurada, la enfermedad
logra establecerse. Esta conclusión sugiere que el refuerzo de la respuesta
inmune del paciente puede proporcionar una medida para la prevención
o el control del cáncer.
Aunque en la actualidad se dispone
de muchas evidencias sobre la respuesta contra las células cancerosas,
el mecanismo de acción exacto aún no ha sido completamente esclarecido.
Se ha identificado una serie
de antígenos contra los que se ha evidenciado respuestas inmunes y se
sabe que se requiere de mecanismos de citotoxicidad producidos por células
T citotóxicas o células killer además de procesos dependientes
de anticuerpos. Las células tumorales evaden estos mecanismos.
Por otra parte, las células
tumorales son capaces de secretar factores solubles que ejercen efectos inmunosupresores,
hecho que inhibe la actividad de ciertos linfocitos T y diminuye la actividad
de los macrófagos y de los linfocitos T citotóxicos.
La implementación de la llamada inmunoterapia a través de la aplicación de citoquinas o interferón tiende a aumentar la actividad citotóxica directa.Asimismo, se está intentando aumentar la capacidad de las células tumorales a desarrollar una respuesta inmune efectiva mediante la transferencia de genes activadores de la respuesta. Los últimos avances tienden a desarrollar productos que, mediante la aplicación de técnicas de DNA recombinante permitan el desarrollo de vacunas potenciales contra el cáncer.
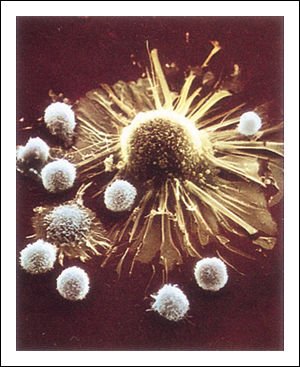
La destrucción exitosa de una célula cancerosa por linfocitos T citotóxicos (a).
a) El reconocimiento de la célula cancerosa como anormal depende de la presencia de neoantígenos expuestos en su superficie en conjunción con los antígenos CMH de clase I.
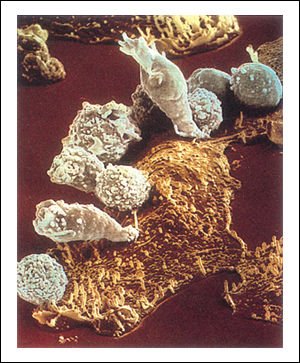
La destrucción exitosa de una célula cancerosa por linfocitos T citotóxicos (b).
b) y c) Cuando los linfocitos citotóxicos comienzan a dañar la
membrana de la célula cancerosa su forma cambia.
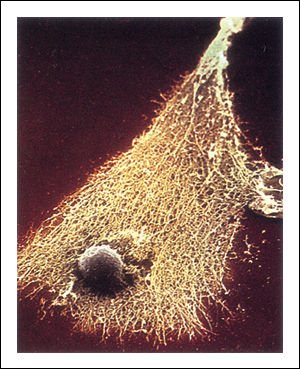
La destrucción exitosa de una célula cancerosa por linfocitos T citotóxicos (c).
Trasplantes de tejido
Si se toma piel de una parte
del cuerpo de un paciente quemado y se injerta en el área quemada, el
nuevo tejido se suelda al área expuesta, es invadido por vasos sanguíneos-
y el tejido crece y se extiende. Si un injerto de piel se toma de otro individuo,
a menos de que se trate de un gemelo idéntico del paciente, las etapas
iniciales de cura y vascularización ocurren pero luego, entre el quinto
y el séptimo día, una gran cantidad de leucocitos se infiltran
en el tejido trasplantado y el paciente muere. Las células que se infiltran
son principalmente linfocitos T y macrófagos que han sido activados por
el reconocimiento de antígenos presentes en las células que provienen
de otro individuo de la misma especie. El descubrimiento y la identificación
de los antígenos del complejo mayor de histocompatibilidad (CMH) actualmente
está haciendo posible acentuar la semejanza entre el dador y el receptor
en los trasplantes de órganos.
A los receptores de trasplantes
generalmente se les suministran drogas que suprimen la respuesta inmune. Sin
embargo, dado que la infección es una complicación importante
entre los pacientes receptores, la supresión general de la respuesta
inmune no es, obviamente, una solución ideal.
Los trasplantes de tejidos más
frecuentes en la práctica médica son las transfusiones de sangre.
Existen grupos sanguíneos principales: A, B, AB y 0.
Los eritricitos humanos, a diferencia
de las células con núcleo, no tienen antígenos CMH en su
superficie. En lugar de esto, exhiben antígenos únicos, codificados
por un gen completamente diferente que, en la población humana, tiene
tres alelos (A, B y 0). Los principales grupos sanguíneos están
definidos por estos antígenos y por la presencia de anticuerpos en el
plasma
Los alelos A y B son codominantes,
mientras que el alelo 0 es recesivo.
Si una persona recibe una transfusión que contenga glóbulos rojos que llevan un antígeno no propio, los anticuerpos en su plasma pueden reaccionar con estas células haciendo que se aglutinen y sean fagocitadas por el sistema del reticuloendotelial.

Reacciones graves, y a veces mortales, pueden ocurrir después de transfusiones de sangre de un tipo diferente de la del receptor.
Estas reacciones se producen
por la aglutinación y destrucción de los glóbulos rojos
del donante causadas por la reacción con los anticuerpos presentes en
la sangre del receptor. Las reacciones del grupo sanguíneo en las transfusiones
pueden demostrarse igualmente bien en tubos de ensayo, como se muestra en este
esquema. El plasma sanguíneo en donde se produce la aglutinación,
tiene anticuerpos naturales contra la sangre del dador.
Se han identificado antígenos
adicionales en la superficie de los glóbulos rojos. Entre los más
importantes de estos antígenos está el factor Rh, que recibe su
nombre de los monos Rhesus, en los cuales se hizo la investigación que
condujo a este descubrimiento.
Patologías del sistema
inmune
Habitualmente, el sistema inmune
puede distinguir entre lo propio y lo no propio. Sin embargo, este reconocimiento
ocasionalmente falla y el sistema inmune ataca a las células del cuerpo
dando lugar a una patología de tipo autoinmune.
En algunas de las enfermedades
hasta hoy reconocidas, el proceso es mediado por la producción de "autoanticuerpos"
que reconocen proteínas de la superficie celular. Otras veces, la enfermedad
autoinmune está mediada por linfocitos T autorreactivos. Algunas de las
enfermedades autoinmunes son la Miastenia gravis, el Lupus eritematoso sistémico
y la anemia hemolítica autoinmune.
El tratamiento médico
de estas patologías tiende a controlar la respuesta inmune de manera
general, por lo que se utilizan drogas antiinflamatorias e inmunosupresoras.
Se cree que los tratamientos que puedan inhibir los clones autorreactivos serán
la terapia del futuro.
En algunas oportunidades, el
sistema inmune reacciona frente a sustancias aparentemente inofensivas. La fiebre
del heno y otras alergias son el resultado de la respuesta inmune al polen,
al polvo o a algunos alimentos, que son antígenos débiles a los
cuales la mayoría de los individuos no reaccionan. En otros individuos,
la respuesta es de tal magnitud que resulta nociva para el organismo; se la
ha denominado reacción de hipersensibilidad o alergia.
En un primer contacto con el
antígeno, no se manifiesta ningún tipo de reacción pero,
tras una segunda exposición a ese antígeno, se pone de manifiesto
una reacción inflamatoria rápida.
Los sistemas antigénicos
responsables son denominados alergenos y en condiciones normales no inducen
ninguna respuesta. La exposición al alergeno origina una respuesta con
activación de ciertos linfocitos T colaboradores. Éstos activan
a los linfocitos B, con la producción de anticuerpos IgE por células
plasmáticas específicas y formación de las células
de memoria. Al reexponerse al mismo antígeno, se forman más anticuerpos
IgE. Estos anticuerpos permanecen poco tiempo en circulación. La unión
posterior del antígeno a estos anticuerpos unidos provoca cambios en
la membrana celular con la liberación de diversas mediadores que inducen
una respuesta inflamatoria.
Pueden resultar reacciones sistémicas
si los mastocitos y otros basófilos descargan sus productos químicos
en la circulación, lo que provoca una dilatación de los vasos
sanguíneos lo que, a su vez, lleva a una caída potencialmente
peligrosa en la presión sanguínea y a la contracción de
la musculatura lisa de los bronquiolos. Este síndrome se conoce como
"shock" anafiláctico.
Los antihistamínicos
contrarrestan el efecto de la histamina por bloqueo de los receptores específicos.
Así, suprimen parte de los síntomas de una reacción alérgica.
Existe un grupo heterogéneo
de enfermedades surgidas como consecuencia de defectos del sistema inmune denominadas
inmunodeficiencias. Las inmunodeficiencias pueden ser originadas por defectos
genéticos o pueden ser producidas por una causa adquirida, como por ejemplo,
la infección por el virus HIV, agente causal del síndrome de inmunodeficiencia
adquirida (SIDA) o como consecuencia de malnutrición e incluso de estrés
o depresión.
Los individuos portadores de
una inmunodeficiencia tienden a padecer infecciones en forma repetida.
El SIDA fue identificado por primera vez en 1981. En tres años se aisló y caracterizó al virus responsable. Desde entonces, sus efectos principales sobre el sistema inmune han sido determinados, se han identificado sus posibles orígenes y se han constatado sus modos de transmisión. El virus del SIDA es un retrovirus conocido formalmente como virus de la inmunodeficiencia humana (HIV) y es un virus particularmente complejo.
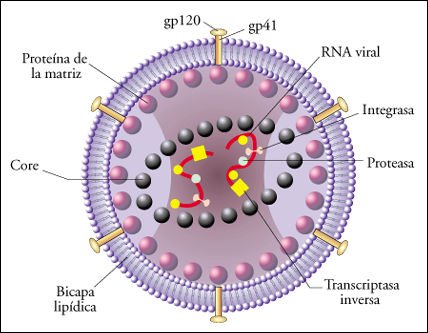
Estructura del virus HIV.
El núcleo interno contiene dos moléculas de RNA, acompañadas
por dos o más moléculas de la enzima transcriptasa inversa. Rodeando
al core se encuentran envolturas formadas por dos proteínas distintas.
Éstas, a su vez, están rodeadas por una bicapa lipídica
que deriva de la membrana celular de la célula hospedadora en la que
el virus previamente se replicó. Atravesando esta membrana se encuentran
las glucoproteínas de superficie que se unen a receptores celulares y
permiten el ingreso del virus a la célula hospedadora.
El retrovirus responsable del
SIDA invade y destruye las células T colaboradoras, dejando al sistema
inmune de la víctima incapaz para responder a otras infecciones o a células
malignas. En las etapas finales de la enfermedad, invade a otras células
y tejidos del cuerpo, incluidos los del sistema nervioso. El virus HIV está
presente en altos niveles en la sangre y en el semen de los individuos infectados
y se transmite por contacto sexual (heterosexual u homosexual, oral, vaginal
o anal) y a través del intercambio de sangre o de productos de la sangre.
Las secuencias de nucleótidos
del RNA del virus HIV ya han sido determinadas, y se identificaron también
secuencias para las varias proteínas de su cubierta. Se está utilizando
tecnología de DNA recombinante para crear vacunas sintéticas contra
el virus. Sin embargo, los anticuerpos sintetizados por los linfocitos B son
inefectivos para controlar la infección y esto sugiere que la obtención
de una vacuna realmente protectora puede ser extraordinariamente difícil.
La tarea también se complica por la alta tasa de mutación de los
genes que codifican la parte clave de la cubierta proteica.
Las pruebas para detectar los
anticuerpos contra HIV suministraron un modo de identificar la sangre de donantes
portadores del virus y aseguran ahora un alto nivel de protección para
el suministro de sangre. En consecuencia, el número de nuevos casos de
SIDA en los receptores de transfusiones y en los hemofílicos ha disminuido.
La dispersión del virus en las poblaciones de homosexuales también
se ha reducido de manera significativa, en parte, porque los individuos más
susceptibles ya habían contraído la enfermedad y, tal vez lo más
importante, a raíz de campañas educativas y cambios en las prácticas
sexuales. Actualmente, el incremento mayor de nuevos casos está ocurriendo
entre los drogadictos que comparten agujas, sus parejas sexuales y sus hijos.
En los últimos años,
se han obtenido importantes logros en relación con los tratamientos.
En la actualidad, la terapia está dirigida fundamentalmente al uso combinado
de inhibidores de proteasas junto con dideoxinucleósidos. Los dideoxiderivados
inhiben la transcriptasa inversa impidiendo la producción del DNA necesario
para la integración del material genético del virus al genoma
de la células del hospedador.
Se han combinado las terapias
mencionadas con agentes antivirales, combinación que ha permitido una
reducción de la carga viral del paciente en un 99% en un corto tiempo.
Esto ha alentado a los investigadores a pensar que la enfermedad podría,
en un futuro no muy lejano, convertirse de una enfermedad mortal en una infección
crónica. Sin embargo, la enorme capacidad de mutación que presenta
el virus hace difícil predecir el mañana. Otro hallazgo importante
ha sido la identificación de diversos inhibidores de quimoquinas sobre
la capacidad de infección del HIV, lo que permitiría el desarrollo
de nuevas estrategias inmunoterapéuticas.
Aplicaciones inmunoterapéuticas
La vacunación explota
la capacidad del sistema inmunológico de generar una respuesta inmune
frente a alguna forma alterada de un patógeno determinado. Este procedimiento
permite el desarrollo de células con memoria inmunológica que
confieren protección a lo largo de toda la vida del organismo vacunado.
Diferentes tipos de vacunas
han sido utilizadas a lo largo del tiempo. Las bacterias y virus muertos han
sido y continúan siendo utilizadas en determinadas circunstancias. Las
vacunas creadas con la utilización de microorganismos vivos atenuados
resultan ser mejores inmunógenos que las anteriores, pero presentan el
riesgo de la reversión del patógeno alterado a la forma virulenta
y son, por lo tanto, peligrosos.
Cada vez es más frecuente
el uso de la tecnología del DNA recombinante para obtener proteínas
que generan una respuesta inmune.
Se están desarrollando
las llamadas vacunas a DNA. Para ello, los genes que codifican proteínas
de interés son insertados en plásmidos adecuados, los que luego
son inyectados dentro de células musculares de manera que la proteína
se puede expresar en forma prolongada. El procedimiento produce
una buena respuesta humoral como también una especial estimulación
de los linfocitos T § citotóxicos.
La posibilidad de transferir
genes con el fin de reemplazar, corregir o modificar la acción de otros
genes permite pensar en la posibilidad de mejorar una gran variedad de enfermedades,
entre ellas el cáncer